Multicenter - het toevoegen van een deelnemend centrum
Bij multicenter studies kunnen de deelnemende centra geregistreerd worden. Dit kan alleen indien de studie is aangemerkt als "Multicenter, verrichtend centrum".
Toevoegen deelnemend centrum:
- Ga naar het Studies menu;
- Open de studie;
- Ga naar het Deelnemende centra tabblad;
- Klik op de Toevoegen deelnemend centrum knop;
- Vul het formulier in;
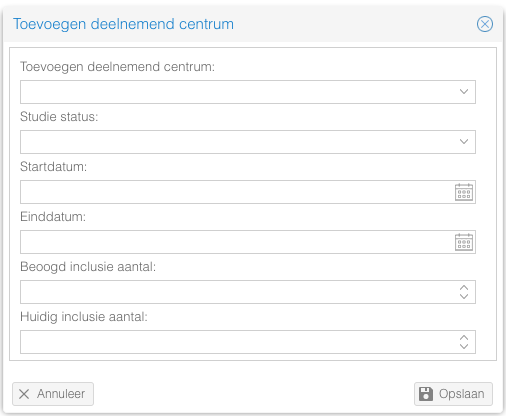
- Klik op de Opslaan knop.
Het deelnemend centrum is nu toegevoegd.
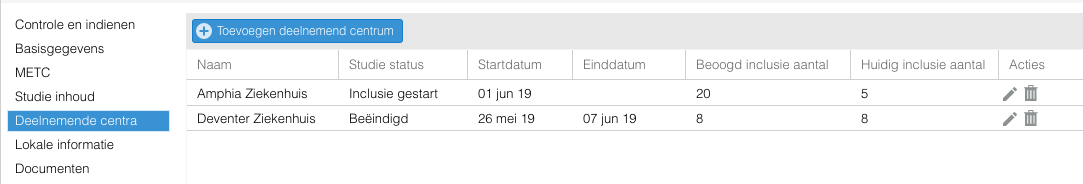
De lijst met deelnemende centra word beheerd door de Admin(s) van de Castor SMS omgeving.