Rollen en rechten: Automatisch rollen aanmaken (gekoppeld aan deelnemende afdelingen en goedkeuringsaanvragen)
Er zijn 2 manieren om nieuwe rollen aan te maken: handmatig en automatisch. De rollen waarbij automatisch rechten worden gemaakt zijn van toepassing op de deelnemende afdelingen en goedkeuringsaanvragen. Dit onderdeel van de handleiding gaat over het maken en beheren van automatische rollen (gekoppeld aan deelnemende afdelingen en goedkeuringsaanvragen).
Klik hier om naar de handleiding over de manuele rollen te gaan.
Automatisch aanmaken van rollen: deelnemende afdelingen
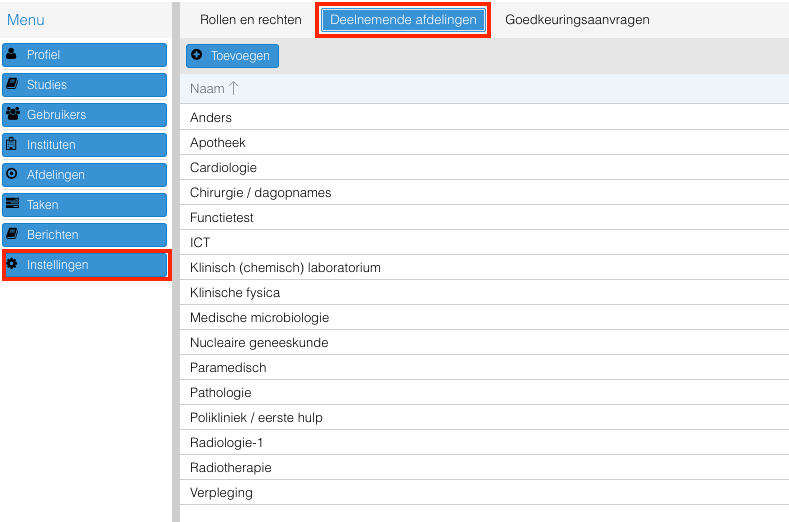
- Ga naar het Instellingen menu;
- Ga naar het Deelnemende afdelingen tabblad;
- Klik op Toevoegen;
- Vul de Engelse en Nederlandse naam in van de optiegroep en tevens gebruikersrol en klik op Opslaan.
.png)
De deelnemende afdeling is toegevoegd. Dit houdt in dat:
- In het Deelnemende afdelingen tabblad van een studie deze nieuwe keuzeoptie is toegevoegd;
- In het Gebruikersmenu deze rol is toegevoegd (Engelse naam) met de volgende standaard rechten:
- Inzage studie waarbij de Deelnemende afdeling is toegevoegd;
- Documenten tabblad: Bestanden kunnen downloaden, toevoegen en archiveren;
- Deelnemende afdelingen tabblad: Data van de eigen deelnemende afdeling kunnen bewerken;
- Factuuradressen tabblad: Factuuradressen kunnen toevoegen en bewerken.
Automatisch aanmaken van rollen: goedkeuringsaanvragen
- Ga naar het Instellingen menu;
- Ga naar het Goedkeuringsaanvragen tabblad;
- Klik op Toevoegen;
.png)
- Vul de Engelse en Nederlandse naam in van de optiegroep en tevens gebruikersrol en klik op Opslaan.
.png)
De goedkeuringsaanvraag is toegevoegd. Dit houdt in dat:
- In het Goedkeuringsaanvragen tabblad van een studie deze nieuwe keuzeoptie is toegevoegd;
- In het Gebruikersmenu deze rol is toegevoegd (Engelse naam) met de volgende standaard rechten:
- Inzage studie waarbij de goedkeuringsaanvraag is toegevoegd;
- Documenten tabblad: bestanden kunnen downloaden; toevoegen en archiveren;
- Goedkeuringsaanvragen tabblad: de status van de eigen goedkeuringsaanvraag aanpassen, én het toevoegen van een nieuwe goedkeuringsaanvraag
- Dashboard menu: inzage in de de goedkeuringsaanvragen weergave van de dashboard.
Verwijderen van een deelnemende afdeling of goedkeuringsaanvraag
Een deelnemend centrum of goedkeuringsaanvraag kan verwijderd worden door op het x symbool te klikken, of middels rechtermuisknop.
.png)
Het is niet mogelijk om een deelnemende afdeling of goedkeuringsaanvraag te verwijderen als:
- deze optie in gebruik is door een studie;
- deze rol is toebedeeld aan een gebruiker.